9.2. Уравнения состояния и закономерности движения газа
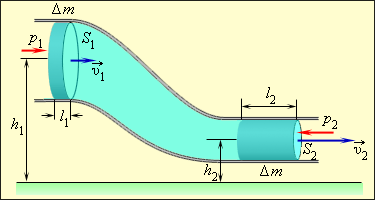
Расход газа — это количество газа, прошедшего через поперечное сечение трубопровода за единицу времени. Вопрос в том, что принять за меру количества газа. В этом качестве традиционно выступает объем газа, а получаемый расход называют объемным.




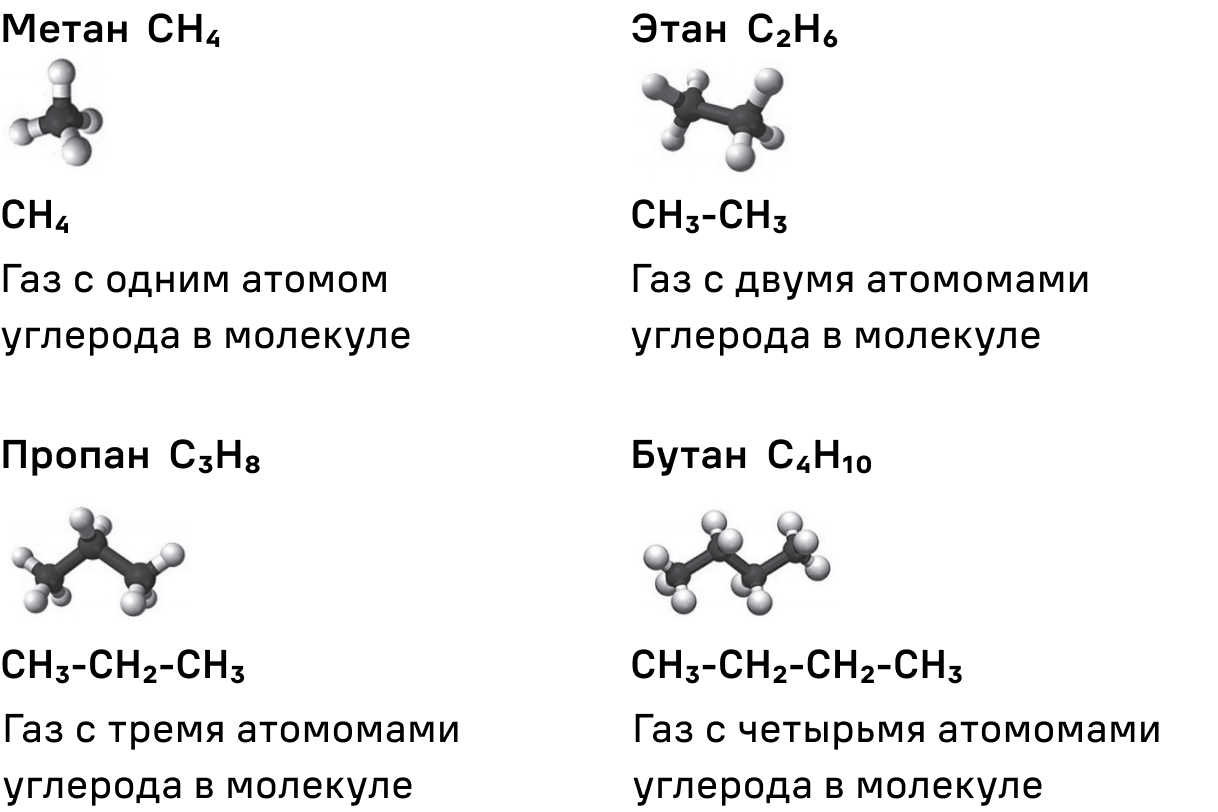
Агрегатное состояние — состояние вещества, характеризующееся определёнными качественными свойствами — способностью или неспособностью сохранять объём и форму, наличием или отсутствием дальнего и ближнего порядка и другими. Изменение агрегатного состояния сопровождается скачкообразным изменением свободной энергии, энтропии, плотности и других основных физических свойств. В современной физике выделяют следующие агрегатные состояния: твёрдое тело, жидкость, газ, плазма ранее им соответствовали 4 стихии первоэлементы : Земля, Вода, Воздух, Огонь.
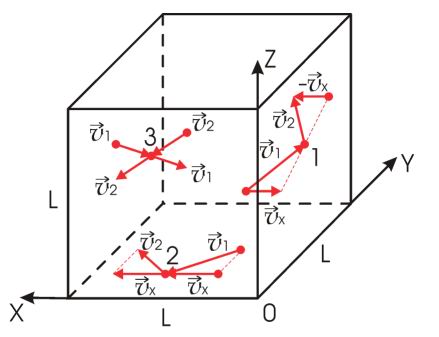
- В отличие от жидкости и твердого тела, где молекулы находятся на близких расстояниях и связаны друг с другом значительными по величине силами притяжения и отталкивания, взаимодействие молекул в газе проявляется лишь в короткие моменты их сближения столкновения. При этом происходит резкое изменение величины и направления скорости движения сталкивающихся частиц.
- Газы , вещества в агрегатном состоянии, характеризующемся слабым взаимодействием составляющих вещество частиц по сравнению с их средней кинетической энергией , в результате чего газы заполняют весь предоставленный им объем. Газы, как и нормальные обычные жидкости, макроскопически однородны и изотропны при отсутствии внеш.
- Запах газа коррелирует с концентрацией сероводорода. Избыточному скоплению газов способствуют заглатывание воздуха аэрофагия и диффузия из кровотока в просвет кишечника.

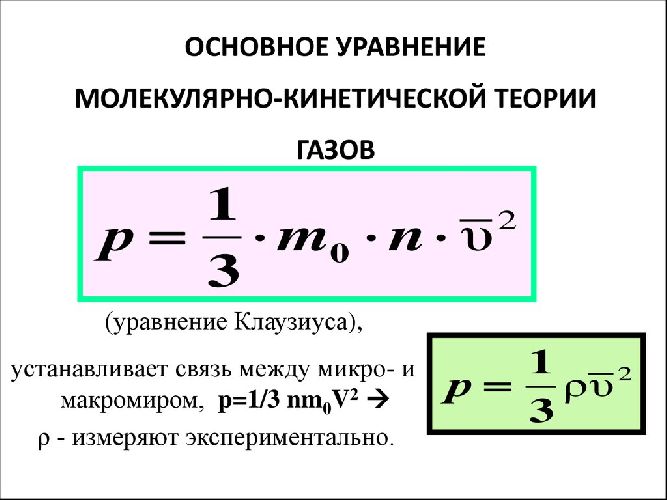
![Основные положения молекулярно-кинетической теории [ М Г Т У ]](http://profil.adu.by/pluginfile.php/3506/mod_book/chapter/9209/01.jpg)

.jpg)



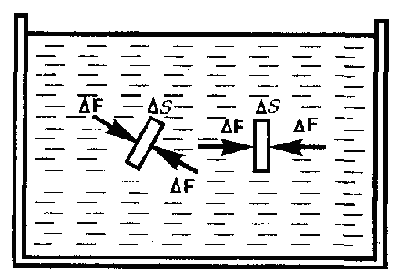

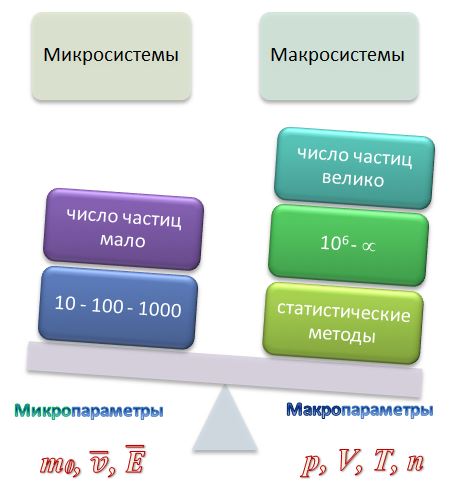
ГЛАВА 2 2. Основные положения молекулярно-кинетической теории. Метод описания свойств сложных объектов, например термодинамических систем, через свойства элементарных их составляющих, был впервые использован в древней Греции.